Je posterais ma réponse pour Juin 2007 Q2 plutard mais as tu penser au changement d'état lors de ta détente isentropique ?
Normalement tu devrais avoir un changement de phase lors de la sortie de la dernière turbine et c'est la que ça coince tu auras de la vapeur humide et non plus de la simple vapeur d'où un titre que tu dois calculer !!! Je le fais pour le soir ! bonne chance pour rectifier ta réponse.
EDIT1:
Donc si j'ai bien compris ta question c'est la question Janvier 2007 Q2.
Donc nous avons les données suivantes : Détente adiabatique dans une turbine, Pin=P1= 3 10^6 Pa ,Tin=T1= 400°C ,Pout=P2= 50 10^3 Pa, Rendement isentropique= 66,7%
--------------
Inconnues:
Tout'=T2'?
Analysons ces données, nous voyons que le cycle est irréversible ! Pq? car nous avons un rendement isentropique donc Le prof veut une température out irréversible, nous allons donc chercher T réversible pour trouver T(irrév.) comment ?
Partie1: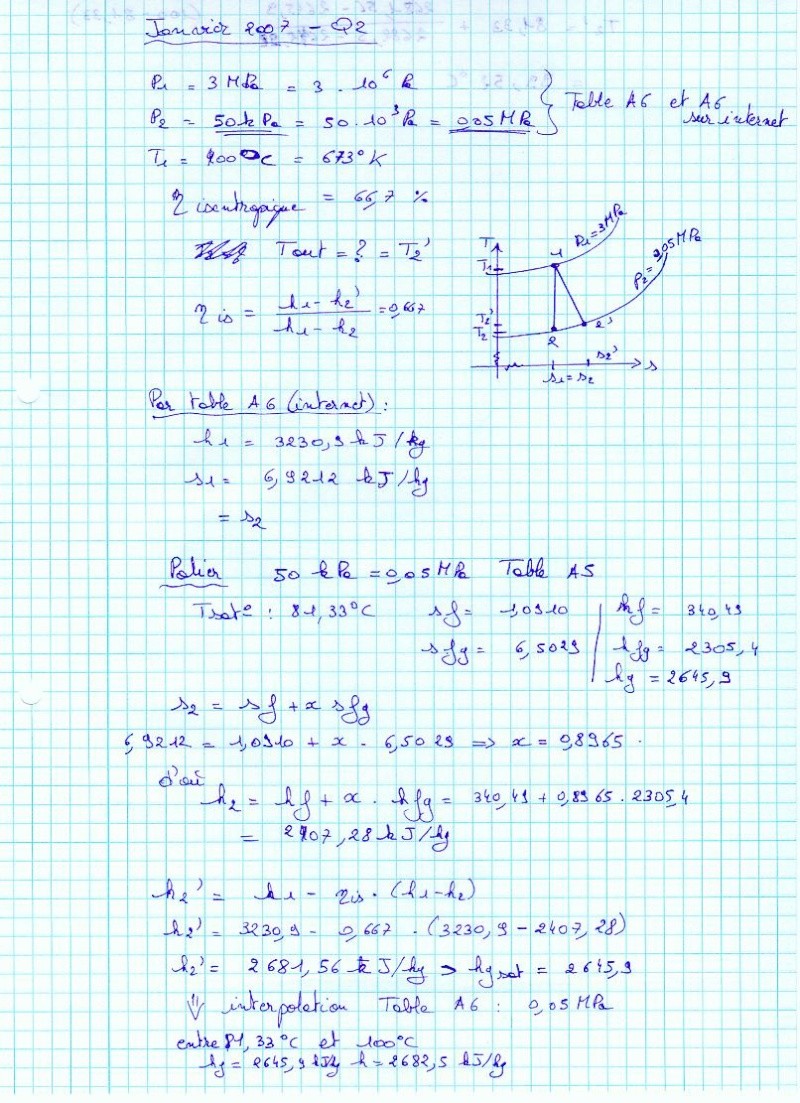
Partie2:
pour la table A6 d'internet voici l'adresse: http://imrl.usu.edu/thermo/Blue/frames/a6f.htm
EDIT2: WArning m'a fait remarqué que j'avais fait une erreur lors de ma deuxième interpolation pour trouver T'2, en prenant la table A6 à 0,5MPa à la place de 0,05MPA Veuillez m'en excuser pour ce désagrément ! A présent c'est jsute dans le Edit1!
Normalement tu devrais avoir un changement de phase lors de la sortie de la dernière turbine et c'est la que ça coince tu auras de la vapeur humide et non plus de la simple vapeur d'où un titre que tu dois calculer !!! Je le fais pour le soir ! bonne chance pour rectifier ta réponse.
EDIT1:
Donc si j'ai bien compris ta question c'est la question Janvier 2007 Q2.
Donc nous avons les données suivantes : Détente adiabatique dans une turbine, Pin=P1= 3 10^6 Pa ,Tin=T1= 400°C ,Pout=P2= 50 10^3 Pa, Rendement isentropique= 66,7%
--------------
Inconnues:
Tout'=T2'?
Analysons ces données, nous voyons que le cycle est irréversible ! Pq? car nous avons un rendement isentropique donc Le prof veut une température out irréversible, nous allons donc chercher T réversible pour trouver T(irrév.) comment ?
Partie1:

Partie2:

pour la table A6 d'internet voici l'adresse: http://imrl.usu.edu/thermo/Blue/frames/a6f.htm
EDIT2: WArning m'a fait remarqué que j'avais fait une erreur lors de ma deuxième interpolation pour trouver T'2, en prenant la table A6 à 0,5MPa à la place de 0,05MPA Veuillez m'en excuser pour ce désagrément ! A présent c'est jsute dans le Edit1!
Dernière édition par moderateur002 le Lun 4 Jan - 18:14, édité 5 fois





